АЦИЛОИНОВАЯ КОНДЕНСАЦИЯ, образование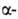 гидроксикетонов
(ацилоинов) восстановлением эфиров алифатич. моно- или дикарбоновых к-т,
напр.:
гидроксикетонов
(ацилоинов) восстановлением эфиров алифатич. моно- или дикарбоновых к-т,
напр.:
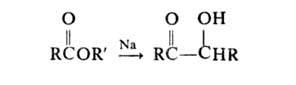
А.к. эфиров монокарбоновых к-т осуществляется двумя путями:
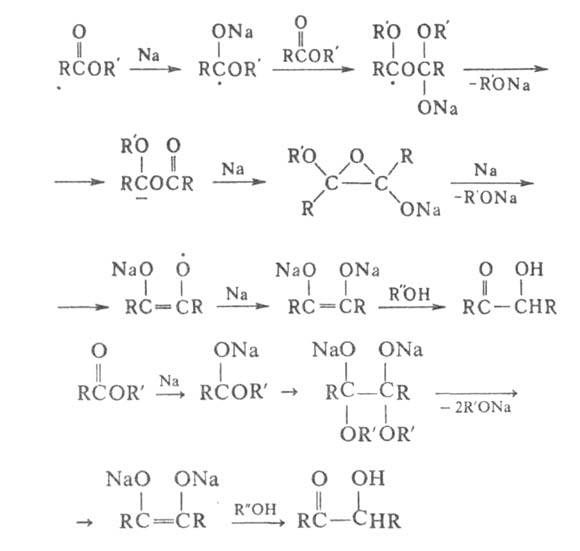
Сложный эфир нагревают с Na (мольное соотношение 1:2) в бескислородной атмосфере в инертных р-рителях, напр. в бензоле, толуоле, ксилоле. Применение вместо Na жидкого сплава его с К позволяет проводить процесс при комнатной т-ре. Для повышения выхода ацилоинов в р-ции используют (CH3)3SiCl; образующиеся при этом бис-триметилсилиловые эфиры ендиолов легко выделяются и при взаимод. со спиртом образуют ацилоины. При осуществлении А.к. без (CH3)3SiCl получаются побочные продукты-1,2-дикетоны, кетоны, а также вещества, синтезирующиеся в результате конденсации Дикмана и Клайзена.
С помощью А. к. можно получать с хорошими выходами ациклич. ацилоины с R от СН3 до С22Н45. Р-ция с участием эфиров двух разных монокарбоновых к-т практически не осуществляется.
Из эфиров дикарбоновых к-т в условиях, при к-рых происходит А. к. монокарбоновых
к-т, образуются циклич. ацилоины:
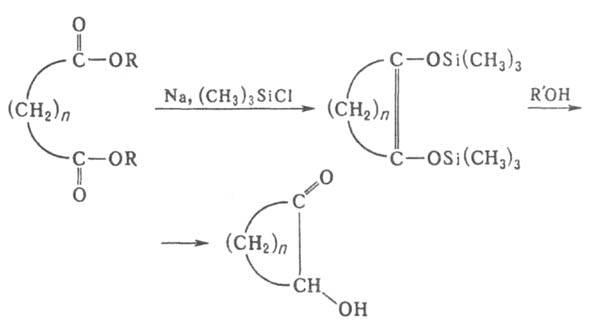
Таким путем можно получить ацилоины, содержащие в цикле от 4 до 42 атомов
С. Эту же реакцию используют для синтеза макроциклических гетероциклических
ацилоинов и ацилоинов с конденсированными циклами, напр.:
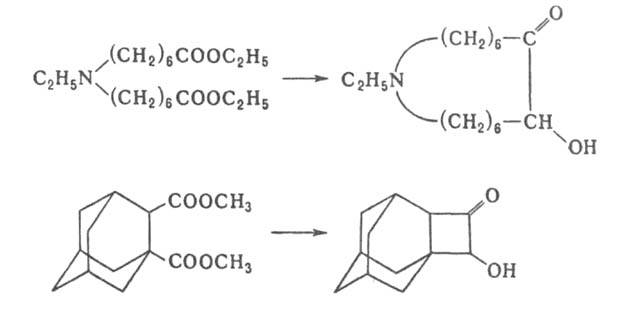
В результате А. к. эфира дикарбоновой к-ты, содержащей 34 атома С, в
присут. 34-членного циклоалкана удалось получить катенан. А.к. - промежут.
р-ция при получении макроциклич. углеводородов, макроциклич. и ациклич.
кетонов,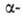 дикетонов
и диолов.
дикетонов
и диолов.
Лит.: Bloomfield J.J. [а.о.], в кн.: Organic reactions, v. 23, N.Y.-L.,
1976, p. 259-403. H. П. Гамбарян.


