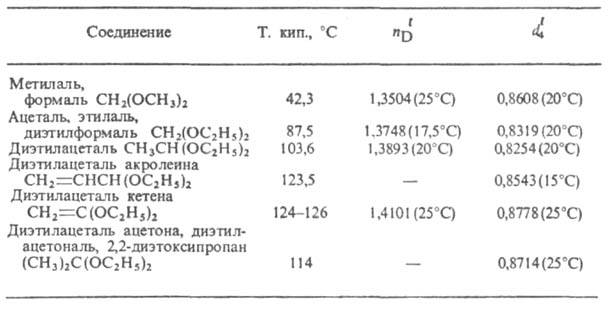
А. и к. - бесцв. жидкости с приятным запахом (см. табл.); раств. в орг. р-рителях, не раств. в воде. В небольших кол-вах содержатся в виноградных винах.
СВОЙСТВА НЕКОТОРЫХ АЦЕТАЛЕЙ И КЕТАЛЕЙ
А. и к. устойчивы в щелочных средах и очень легко гидролизуются в кислых
до альдегидов и кетонов, вследствие чего ацетальную группировку используют
для защиты карбонильной группы при проведении р-ций по др. реакц. центрам
в нейтральной или щелочной среде; напр., получение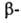 гидроксиальдегидов
из эфиров альдегидокислот:
гидроксиальдегидов
из эфиров альдегидокислот:
См. также Защитные группы.
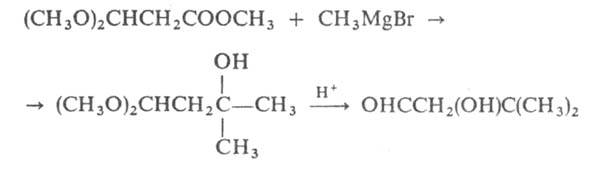
При нагр. А. и к. со спиртами или тиолами происходит полный или частичный
обмен алкоксигрупп на др. алкоксиили алкилтиогруппы:
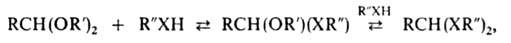
где X = О или S. При взаимод. с первичными аминами, гидразинами или
гидроксиламином в кислой среде образуются соотв. алъдимины (или кетимины),
гидразоны или оксимы, напр.: RCH(OR')2 + R"NH2 ->
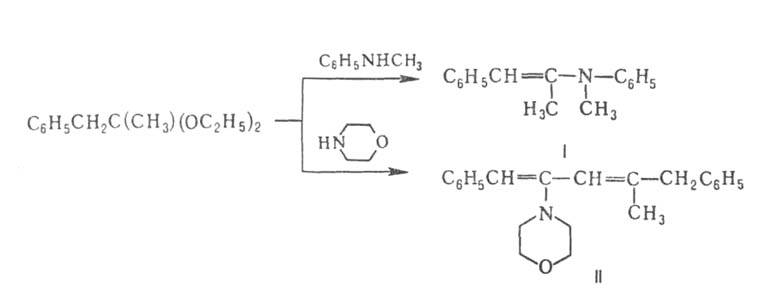
RCH=NR", при р-ции со вторичными аминами в присут. n-толуолсульфокислоты
- енамины (ф-ла I) или диенамины (II):
Для А. и к., имеющих другие функциональные заместители, характерны внутри-
и межмолекулярные циклизации с образованием карбо- или гетероциклич. соединений;
напр., ацетали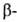 кетоальдегидов
тримеризуются в производные бензола:
кетоальдегидов
тримеризуются в производные бензола:
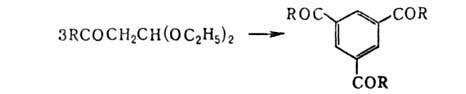
На основе замещенных А. и к. получены производные фурана, кумарина,
тиофена, пиррола, индола, пиридина, хинолина и мн. др. Осн. методы синтеза
А. и к.: 1) взаимод. альдегидов и кетонов (как правило, в присут. кислых
катализаторов) со спиртами, ортоэфирами или тетраалкоксисиланами:
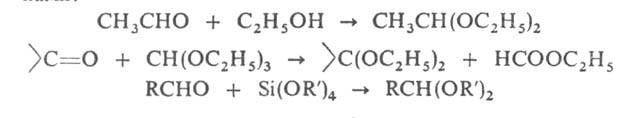
2) р-ции с участием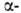 галогенэфиров,
гем-дигалогенидов, гем-диаминов, напр.:
галогенэфиров,
гем-дигалогенидов, гем-диаминов, напр.:
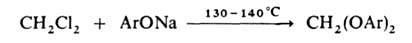
3) присоединение спиртов или ортоэфиров по кратным связям, напр.: СН2=СНОСН3 + СН3ОН -> СН3СН(ОСН3)2.
Последние два метода можно использовать для синтеза разл. карбонильных соед. через стадии получения А. и к. с послед. их гидролизом в кислой среде.
А. и к.-фиксаторы запаха в парфюмерии, флотореагенты (1,1,3-триалкоксипарафины, ацетали акролеина и кротонового альдегида), пластификаторы, моющие средства, смазочные материалы. Некоторые А. и к. обладают биологической активностью; напр., 1,1,3-триэтоксибутан обнаружил высокую противовирусную активность, ацетали хлораля - гербицидное действие, диарилоксиалканы - инсектицидное.
Лит.: Яновская Л. А.. Юфит С. С., Кучеров В. Ф., Химия ацеталей,
М., 1975. В.Г.Граник.


