АЛЛИЛБОРАНЫ, соединения В(III) общей ф-лы I.
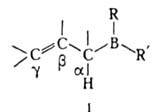
В А. имеется 5 реакционных центров: электроф. атом В, связи В—С, Са—Н, С=С, В—R или В—R' (R, R'-OAlk, Alk, NAlk2 и т.д.). Взаимное влияние атома В и двойной связи отчетливо проявляется в р-циях с участием бор-аллильной системы в целом. Прочность связи В—С в них меньше, чем в алкилборанах (соотв. ~ 285 и ~ 350 кДж/моль).
Различают симметричные (напр., триаллилборан, трикротилборан) и несимметричные, или смешанные, А. К последним относятся, в частности, аллил(диалкил)бораны, диаллил(алкил)бораны, аллил(диалкокси)бораны, три-В-аллилборазол, а также циклим. А. и соед. типа R'XCH=CHCH2BR2, где R = OAlk, SAlk, NAlk2 и R' = Alk, X = О, S.
А. получают переметаллированием, гидроборированием нек-рых алленов,
1,3-диенов, пропаргилгалогенидов и др. методами, напр.:
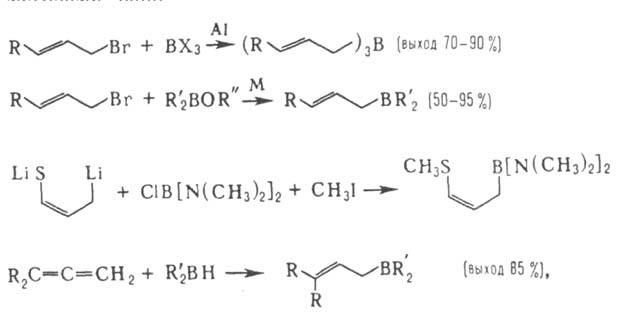
где М = Li, Mg, Al; X = F, Cl, OR; R = H, Alk, Ar, циклоалкил; R' = Alk, Ar, OAlk, NAlk2.
А. легко окисляются и гидролизуются на воздухе, низшие члены ряда самовоспламеняются. Большинство А. расщепляется водой, спиртами, р-рами щелочей и к-т с образованием соответствующих олефинов.
А.-более сильные к-ты Льюиса, чем их алкильные аналоги; они образуют комплексы с аминами, нек-рыми эфи-
рами, сульфидами, фосфинами. При действии RLi получаются бораты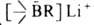 . Комплексообразование - первый акт р-ций А. с нуклеоф. реагентами (Н2О,
ROH, RSH, R2NH, RCHO, RCN, RC=CH и др.).
. Комплексообразование - первый акт р-ций А. с нуклеоф. реагентами (Н2О,
ROH, RSH, R2NH, RCHO, RCN, RC=CH и др.).
Связь В—С разрывается (без перегруппировки) при взаи-мод. А. с Н2О2
(синтез аллильных спиртов), N2CHCOOR' (синтез эфиров RCH=CHCH2CH2COOR'),
циклопропенами или бициклобутаном:
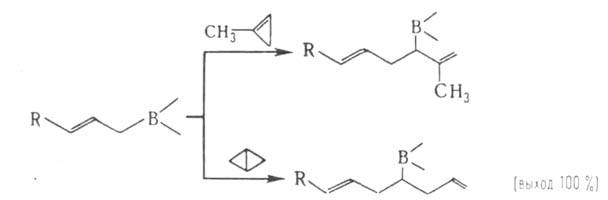
К р-циям А. по двойной связи относятся полимеризация, диеновая конденсация,
гидрирование, присоединение меркаптанов, Вr2, гидридов Ge, Si
и В, напр.:
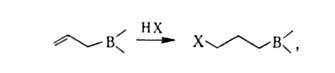
где X = Н, RS, R3Si, R3Ge, R2B.
По связи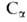 —Н,
активированной бором, идет металлирование (обычно 2,2,5,5-тетраметилпиперидиллитием
с послед. алкилированием).
—Н,
активированной бором, идет металлирование (обычно 2,2,5,5-тетраметилпиперидиллитием
с послед. алкилированием).
В смешанных А. со связью В—XR (X = О, S и др.) легко обменивается заместитель XR.
Все р-ции с участием бор-аллильной системы сопровождаются аллильной
перегруппировкой. К ним относятся: 1. Протолитич. расщепление водой,
спиртами, аминами, меркаптанами, карбоновыми к-тами; используется для синтеза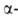 олефинов
через А. 2. Аллилборирование альдегидов, кетонов, сложных эфиров, хинонов,
нитрилов, иминов, виниловых эфиров, циклопропенов и ацетиленов; при этом
В локализуется у нуклеоф. центра кратной связи, а аллильная группа-у электрофильного:
олефинов
через А. 2. Аллилборирование альдегидов, кетонов, сложных эфиров, хинонов,
нитрилов, иминов, виниловых эфиров, циклопропенов и ацетиленов; при этом
В локализуется у нуклеоф. центра кратной связи, а аллильная группа-у электрофильного:
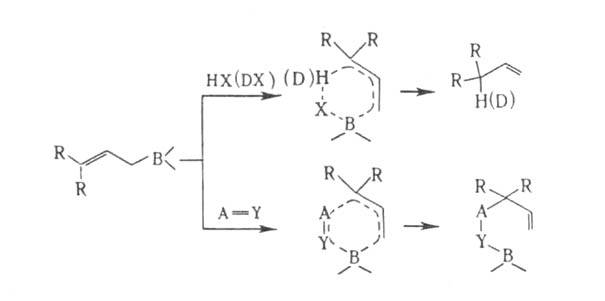
где НХ = Н2О, ROH, RNH2 и др.; A=Y = С=О, С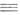 N,
C=N, C=C, С
N,
C=N, C=C, С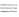 С
или циклопропан.
С
или циклопропан.
Аллилборирование применяется для получения гомоаллильных спиртов и аминов,
1,4-диенов, аллилацетиленов и др., напр.:
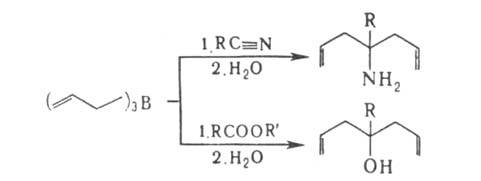
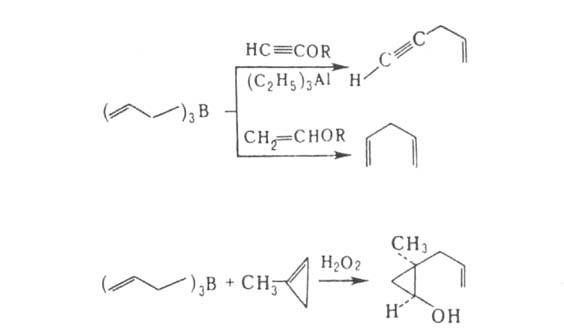
Важнейшая р-ция триаллилборана и его гомологов (триметаллилборана и
др.)-аллилбор-ацетиленовая конденсация, приводящая к соединениям ряда 3-борабицикло[3.3.1]-нон-6-ена:
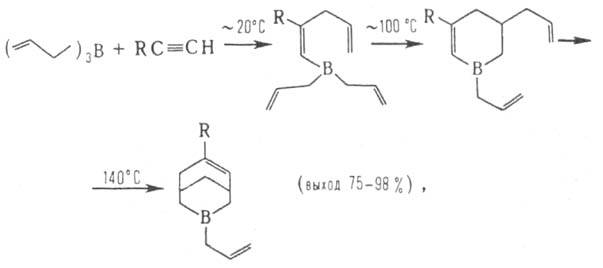
где R = Н, D, Alk, Ar и др.
При взаимод. триаллилборана с алленом получается 3-аллил-7-метилен-3-борабицикло[3.3.1]нонан,
из к-рого был впервые синтезирован 1-бораадамантан:
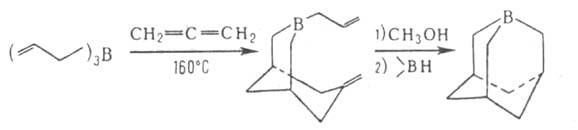
3. Изомеризация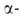 замещенных
А. в термодинамически более устойчивые изомеры, в к-рых В присоединен к
менее замещенному атому С; напр.:
замещенных
А. в термодинамически более устойчивые изомеры, в к-рых В присоединен к
менее замещенному атому С; напр.:
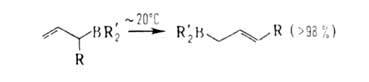
4. Внутримол. перманентная аллильная перегруппировка (ПАП)-быстрая миграция
В от С1 к С3 с одноврем. перемещением двойной связи:
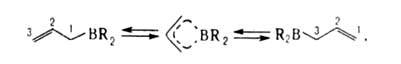
где R-аллил, алкил. При 20 и 200 °С скорость ПАП в триаллилборане соотв. ~ 10 и ~ 104 с -1; энергия активации в зависимости от строения А. варьирует от 21 до 63 кДж/моль. Комплексообразование с аминами, эфирами и сульфидами замедляет ПАП на 2-3 порядка, ПАП не имеет места в эфирах СН2—CHCH2B(OR)2, ангидриде [(СН2=СНСН2)2В]2О и их азотистых аналогах. А.-промежуточные соед. в орг. синтезе.
Лит.: Михайлов Б. М., Бубнов Ю.Н., Борорганические соединения в органическом синтезе, М., 1977; Пелтер А., Смит К., в кн.: Общая органическая химия, пер. с англ., т. 6, ч. 14, М., 1984, с. 233-537. Ю.Н.Бубнов.


