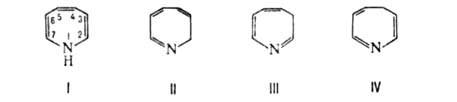
АЗЕПИН (азациклогептатриен). Теоретически возможны 4 изомера:
1Н-А., 2Н-А., ЗН-А. и 4Н-А. (соотв. ф-лы I-IV), однако ни один из них не
выделен. Среди производных А. (для их молекул характерна конформация ванны)
устойчивость уменьшается в ряду: ЗН-А. > 1Н-А. > 4Н-А. > 2Н-А.
Производные 1Н-А. устойчивы при наличии электроноакцепторного заместителя
у атома N. Они легко димеризуются, образуя аддукты в диеновом синтезе с
тетрацианэтиленом (но не реагируют с малеиновым ангидридом и азодикарбоновым
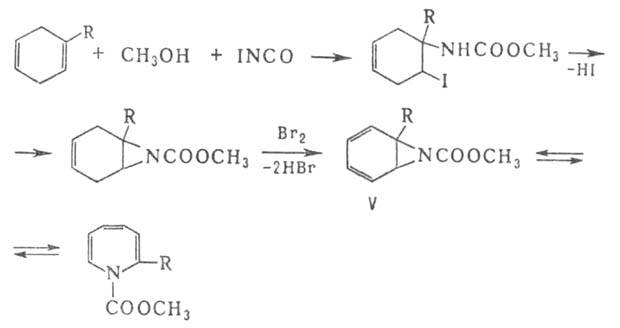
эфиром). Общий метод получения: взаимод. 1,4-циклогексадиенов с иодизсацианатом
и спиртом с образованием производных азаноркарадиена (V), к-рые находятся
в таугомерном равновесии с метоксикарбонил-1Н-азепинами (равновесие обычно
сдвинуто вправо), напр.:
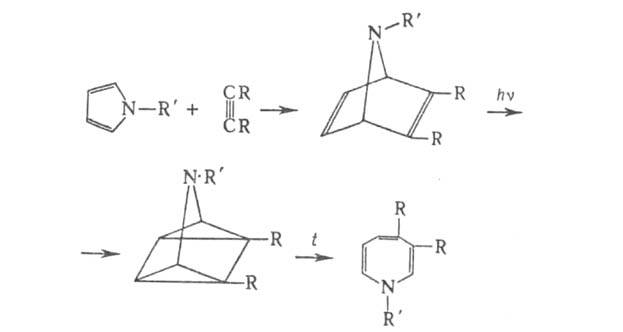
Их синтезируют также взаимод. бензола или его замещенных с нитренами
или термич. перегруппировкой азаквадрицикленов, получаемых фотоизомеризацией
аддуктов диенового синтеза пирролов с ацетиленами:
Все известные производные ЗЯ-А. имеют заместители в положении 2; присоединение
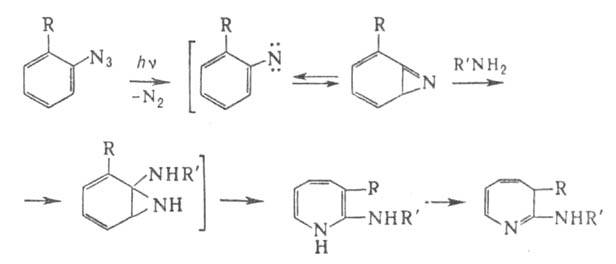
к ним по двойной связи идет гл. обр. в положения 1 и 2. 2-Амино-3Н-А. получают
разложением арилазидов в присут. аминов:
4Н-А. синтезируют из аддуктов ненасыщенных триазинов с дифенилциклопропенами, образующихся в р-ции Дильса-Альдера. Однако при нагр. они превращаются в более устойчивые производные 3Н-А.
Нек-рые производные А., гл. обр. частично гидрированные N-замещенные дибензазепины, используют в медицине как антидепрессанты.
Лит.: Иванский В.И., Химия гетероциклических соединений, М.,
1978, с. 486-93; Общая органическая химия, пер. с англ., т. 8, М., 1985,
с. 708-36. В. Р. Скварченко.


